NAISTなど、水素の分解・合成酵素の反応を制御するスイッチの機構を解明
同成果は、同大 物質創成科学研究科 超分子集合体科学研究室の廣田俊教授、太虎林特任助教、兵庫県立大学 生命理学研究科の樋口芳樹教授、科学技術振興機構 CRESTらによるもの。詳細は、「Angewandte Chemie International Edition」に掲載された。
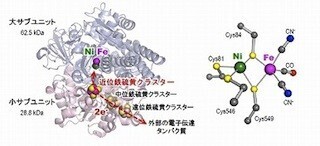
ヒドロゲナーゼは、微生物が有する酵素で水素分子の分解・合成を行う。また、ヒドロゲナーゼは、その活性部位の金属錯体の構成金属の違いから3種類に分類され、それぞれニッケル-鉄ヒドロゲナーゼ、鉄-鉄ヒドロゲナーゼ、鉄ヒドロゲナーゼと呼ばれる。このうち、ニッケル-鉄ヒドロゲナーゼは、最もよく研究されてきた酵素で、大小2つのタンパク質(サブユニット)からなり、ニッケル-鉄活性部位は大きなサブユニット中にある。触媒反応が起こる時、水素分子の分解・合成により、このニッケル-鉄活性部位の配位構造は3つの状態をとる。さらに、触媒反応に関わる電子は小さなサブユニットにある3つの鉄硫黄クラスタを通って外部のタンパク質分子とやりとりされる。
この酵素に光を照射すると、ニッケル-鉄活性部位は3つの状態とは異なる新たな状態になることがわかっていたが、その状態が触媒反応において意味を持つのかは不明だった。
研究グループは、フーリエ変換赤外吸収分光法という分子構造を調べる方法を用い、光照射で生じる状態が触媒反応の中間体であることを突き止めた。そして、3つの鉄硫黄クラスタのうちニッケル-鉄活性部位に最も近いクラスタの電子状態を調べた結果、そのクラスタが還元されている時は触媒反応が進まず、酸化されている時だけ進むことを見出した。つまり、活性部位に最も近い鉄硫黄クラスタがスイッチ役になってヒドロゲナーゼの反応を制御していることを明らかにした。
この酵素による水素分子の分解・合成反応は、現在燃料電池などに利用されている白金などの希少金属触媒と比べて高効率で行われており、今回の成果は、新規の燃料電池や水素合成触媒の開発につながることが期待されているとコメントしている。
提供元の記事
関連リンク
-
「子どもはうるさくても叱らなくていい!元気な証拠じゃない!」しつけをしない迷惑なママ友。子どもを注意するように頼むと⇒「〇〇ちゃんママに怒られるからやめようねw」なぜか悪者扱いされて・・・
-

「ご飯って何度も言ってるけど!?」陣痛中もスマホを見ていた夫との結婚生活…ニュース見てたって言ってるけど本当は…
-
new
【保育園内ダブル不倫】「ばらしたらアンタが家庭を壊すことになるわよ」美人ママの相手は“ママ友の旦那さん”!?秘密を黙っておくが⇒「私の夫、不倫してるの」妻がその事実に気付いて・・・
-

娘の担任と夫の“浮気現場”に突撃!しかし、問い詰めた瞬間⇒ 先生「…勘違いしてません?」妻「え?」
-

“米アカデミー賞ノミネート”山崎エマ監督、小学校30校から撮影NG 母校からも門前払いで製作に費やしたのは計10年

